中国科学家团队,生酮饮食控癌背后的原理,原来是提高了Kbhb水平
- - 阅 1,9408月12号,医学顶刊Nature杂志上,发表了一项最新研究:
这篇研究是华中科技大学薛宇教授、四川大学贾大教授等人在Nature子刊Nature Metabolism上发表的。
研究发现,生酮饮食可以通过赖氨酸β-羟基丁酰化(Kbhb)重塑癌症代谢。①

生酮饮食是一种几乎不吃主食,主要吃肉和优质脂肪的饮食,虽然有很多争议,但是最近几年越来越多的人在研究,践行生酮饮食。
受益的人也越来越多。
今天,我带大家来解读一下这篇文章。
什么是赖氨酸β-羟基丁酰化?
Kbhb是一种新型的组蛋白翻译后修饰,由酮体β-羟基丁酸酯(BHB)诱导而来,可以说酮体是它的前体。
它与脂肪酸氧化代谢、能量代谢调控密切相关。
我们都知道,生酮饮食(高脂肪、极低碳水化合物和充足蛋白质)减少了葡萄糖,导致游离脂肪酸在肝脏中转化为酮体(乙酰乙酸、β-羟基丁酸(β-OHB)和丙酮),其中β-OHB的含量最多。

生酮饮食可以参与多种能量密集型过程,例如脂肪分解、糖异生和蛋白质的热效应,可以使用乙酰乙酸和β-羟基丁酸作为信号调节因子来保持细胞稳态。
早在2016年4月,芝加哥大学赵英明教授团队在 Molecular Cell 期刊发表论文,首次发现Kbhb。②

自发现至今,有关β-羟基丁酰化修饰的研究在众多国际著名期刊上发表,都受到了广泛地关注和认可。
Kbhb蛋白,大量存在于许多核心代谢通路中(包括三大营养物质代谢、谷胱甘肽代谢、一碳代谢、脂肪酸氧化代谢等)。
生酮饮食,重塑癌症代谢
由于只有少数赖氨酸β-羟基丁酰化(Kbhb)位点具有重要功能,因此研究人员开发了一个分层学习框架——预测功能重要的赖氨酸修饰位点(pFunK),用于预测功能重要的赖氨酸修饰位点。
研究人员选择了pFunK预测的6个Kbhb位点,并成功验证了其中5个位点,包括果糖二磷酸醛缩酶B(ALDOB)Lys108。
为了系统研究生酮饮食对肝脏功能的影响,研究人员对进行生酮饮食或非生酮饮食的小鼠的肝脏进行了多组学分析,包括转录组学、蛋白质组学、代谢组学和β-羟基丁酰组学。
研究人员发现,β-羟基丁酰化对肿瘤的发生和发展有着很多重要的代谢途径,例如糖酵解和三羧酸(TCA)循环主要在β-羟基丁酰化水平显著重塑。
实验显示,生酮饮食或在肝细胞癌细胞中补充酮体—β-羟基丁酸(BHB)增加了ALDOB Lys108bhb,抑制ALDOB的酶活性。
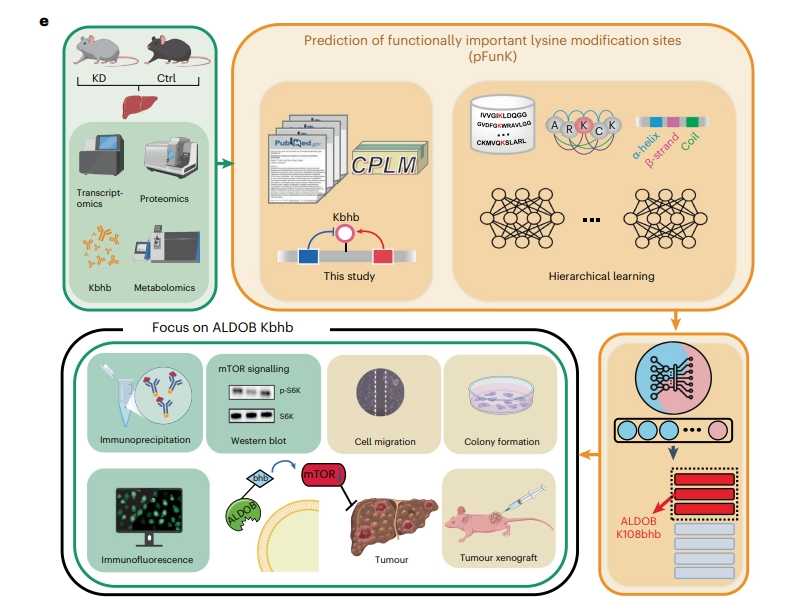
一个模拟Kbhb突变(p.Lys108Gln)减弱了ALDOB的活性及其与底物果糖-1,6-二磷酸的结合,抑制了雷帕霉素靶蛋白(mTOR)信号通路,并显著抑制了癌细胞的增殖。
另外,pFunK还可以扩展到其他类型的赖氨酸酰基化修饰,例如赖氨酸乙酰化(Kac),赖氨酸乳糖化(Kla)和赖氨酸巴豆酰化(Kcr)。
β-羟基丁酰化(Kbhb)的调控作用
主要有以下几个方面:
→影响氨酰-tRNA生物合成、代谢途径
研究发现,经β-羟基丁酸(BHB)诱导后,小鼠胚胎成纤维细胞中840个独特的Kbhb位点被鉴定,其中39个蛋白质上的42个Kbhb位点修饰水平相比于对照组增加了50%以上。
这些上调的Kbhb参与了氨酰-tRNA生物合成、2-氧羧酸代谢、柠檬酸循环、丙酮酸代谢等多种生物途径。
→促进细胞自噬
ULK 是自噬信号通路唯一一个具有丝氨酸/苏氨酸激酶活性的核心蛋白,在自噬溶酶体组装前自噬信号是通过由 ULK1 或 ULK2、FIP200 和 mATG13 组成的 ULK 复合物的活化介导的。
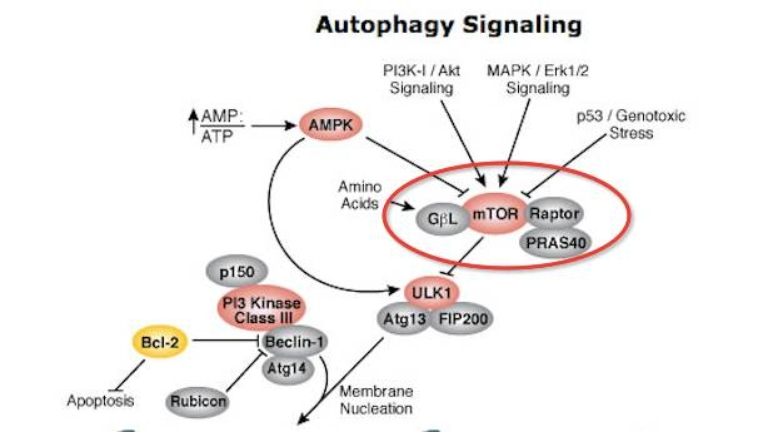
图源www.sohu.com
ULK1作为自噬的起始开关,其激酶活性被抑制后,多个与肿瘤密切相关蛋白的磷酸化水平显著下调,这表明Kbhb可能通过ULK1介导的途径参与调控自噬过程。
→神经保护作用
β-羟基丁酸(BHB)可通过抑制HDAC1/3,上调β样淀粉肽处理的SH-SY5Y细胞TrkA的表达,为防治阿尔茨海默病提供依据。
→减少抑郁发生率
组蛋白3-赖氨酸9-β-羟基丁酰化(H3k9bhb)在抑郁小鼠模型中的改变和治疗后变化,显示了H3k9bhb在抑郁发生中的调控作用,β-羟基丁酸和丙咪嗪治疗可以改善抑郁样行为,并逆转H3k9bhb下降的趋势。
→参与基因表达、能量代谢、DNA损伤修复等生物学过程
稻曲菌中的研究发现,Kbhb修饰参与了结构分子活性调控、氧化还原酶活性、结合、糖酵解、丙酮酸代谢、柠檬酸代谢和丁酸代谢等多个生物学过程。
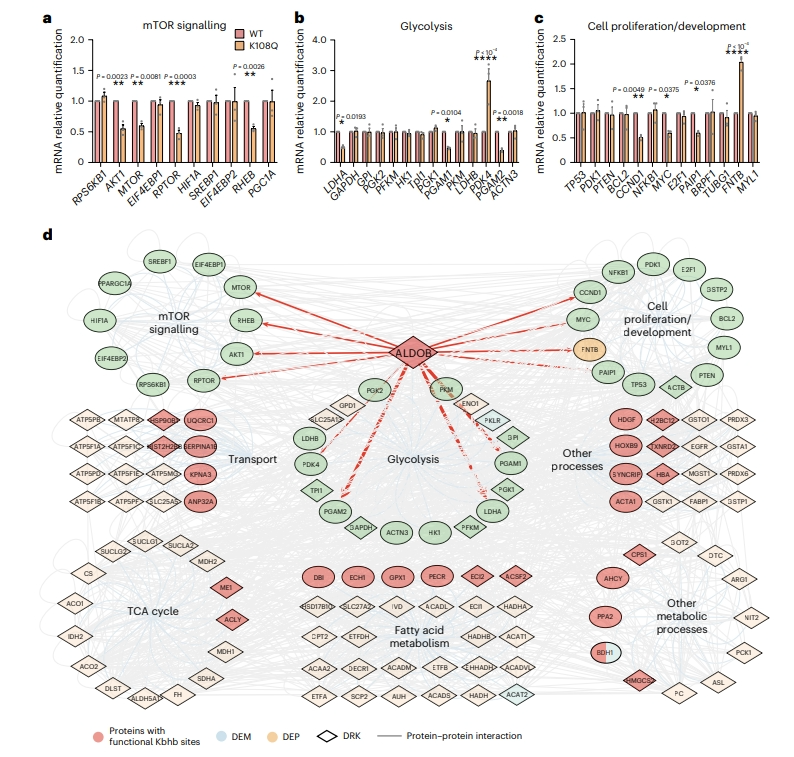
这些蛋白质分为8类,包括mTOR信号传导、细胞增殖/发育、运输、糖酵解、TCA循环、脂肪酸代谢、其他代谢过程和其他过程。
从图可以看出具有潜在功能的Kbhb的蛋白质位点影响各种生物途径,ALDOB在mTOR信号途径、糖酵解和癌症增殖中的具有重要性,显示Kbhb在在癌症代谢的生物学过程中起作用。
当MAPK通路激酶UvSlt2的Kbhb修饰位点突变后,影响了其激酶活性和致病力,这就表示Kbhb修饰在调节蛋白功能和细胞过程中起着关键作用。
2021年的一项研究发现,Kbhb参与到 DNA修复过程,可应用在各种DNA损伤修复模型(癌症放/化疗治疗、辐射损伤等)研究中。③

生酮饮食增加Kbhb?
生酮饮食的核心在于通过限制碳水化合物的摄入,使身体进入“生酮状态”,此时身体开始分解脂肪以产生酮体作为能量来源,这些酮体主要由肝脏产生,可以通过血液运输到大脑和其他组织使用。
由于β-羟基丁酸(BHB)的存在,蛋白质的代谢会发生变化,具体来说,酮体可以减少肌肉蛋白质的分解,从而保护肌肉不被身体过度消耗。
进行生酮饮食时,血浆中的支链氨基酸(如亮氨酸)水平会显著增加,这有助于维持肌肉蛋白的合成和功能。
生酮饮食显著增加了小鼠肝脏中ALDOB的Kbhb水平,但不影响其蛋白水平或Kac水平。

图源
om
此外,ALDOBLys108bhb会抑制其体内和体外的酶活性,Kbhb模拟突变(p.Lys108Gln)会减缓ALDOB活性及其与底物糖酵母二磷酸盐结合,减弱糖酵解和 mTOR信号通路,抑制多种癌症的细胞增殖。
比如2019年的一项研究发现,在经过BHB处理的培养细胞和禁食小鼠的胸腺组织中,抑癌蛋白p53 kbhb的水平显着增加。④

也就是说,BHB能调控p53 kbhb的活性说明酮体与肿瘤之间的联系,为癌症治疗提供有效的治疗靶点。
关键的瘦龙说
生酮饮食辅助控癌,这个不是什么新鲜事了。
之前有一个顶尖的癌症专家,也在声称自己不吃主食,践行生酮饮食。

还有另外一位顶级肿瘤研究学者,他是休斯顿医学博士安德森(MD Anderson)的癌症专家帕特里克·胡(Patrick Hwu)博士,他已经坚持生酮饮食6年。

(Patrick Hwu)本人
他以全脂普通奶油芝士,酸奶油和鳄梨作为主食,还吃绿色蔬菜和花椰菜。
这篇研究发现,赖氨酸β-羟基丁酰化(Kbhb)的作用包括影响氨酰-tRNA生物合成、代谢途径,与自噬过程相关,具有神经保护作用,降低抑郁发生率,以及在基因表达、能量代谢、DNA损伤修复等。
今天分享的最新研究显示,生酮饮食引发的果糖二磷酸醛缩酶B的第108位赖氨酸的赖氨酸β-羟基丁酰化修饰(ALDOB Lys108bhb)在重塑癌症代谢中的关键作用。
进一步证明了ALDOBLys108bhb在抑制mTOR信号通路和抑制癌细胞增殖中的关键作用。
总体而言,这个最新研究不仅统一了该领域许多不同的观察结果,生酮饮食和酮体发挥了抗肿瘤作用,还提供了一种普遍适用的算法来预测功能重要的赖氨酸修饰位点,这对于今后的研究提供了很好的研究工具。
现在越来越多的研究发现,酮体有更多的代谢益处,对大脑的益处,对癌症的好处。
这也带给我们启示,生酮饮食的好处是非常多的,而减肥只是其中的好处之一。
期待有更多关于Kbhb在人类疾病中的功能研究。

====进群、领取食谱,联系瘦龙=====
上百款瘦龙优选的高性价比健康补剂和低碳美食产品任你挑选哦,大家一定要关注哦

长按图片扫码关注哦
瘦龙每天都在公众号(瘦龙健康)这里发布文章,大家一定要关注哦。关注公众号后,请回复食谱二字,获取食谱。
如果你想进群,可以扫描下面的码哦

原文地址:http://www.chinalowcarb.com/kbhb-and-keto-diet/关注微信公众号:『瘦龙健康』,及时获取最新低碳生酮相关的文章,公众号回复减肥,糖尿病,获取相关科普文章推荐。 



